Pengertian, Contoh Larutan Elektrolit dan Non Elektrolit
Penulis Taufiq Firmansah | Ditayangkan 29 Jul 2019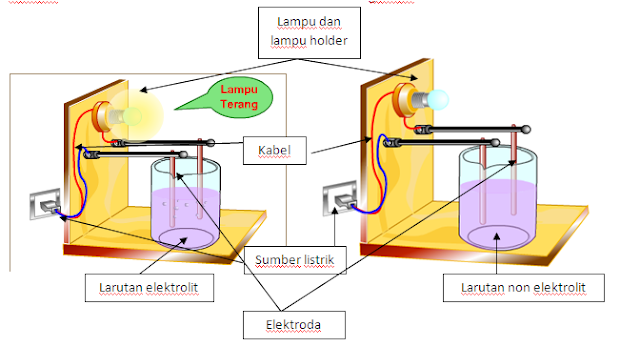
Larutan elektrolit dan non elektrolit - Image from : pelajaranonlinesekolah.com
Tahu nggak berdasarkan gaya hantaran listrik, kita bisa menentukan larutan elektrolit dan non elektrolit lho.
Larutan elektrolit dan non elektrolit adalah campuran homogen antara zat terlarut dan pelarut.
Tahukah anda larutan apa saja yang termasuk larutan elektrolit dan non elektrolit lengkap.
Untuk itu wajib baca akan memberi tahu larutan elektrolit dan non elektrolit beserta contohnya.
Pengertian Larutan Elektrolit
Larutan elektrolit adalah suatu zat yang larut ke dalam bentuk ion-ion, ketika zat yang dilarutkan kedalam air akan berubah menjadi ion dan ion tersebut dapat menghantarkan arus listrik.Berdasarkan pada daya hantar larutan elektrolit dibagi menjadi dua, elektrolit kuat yang memiliki daya hantar yang besar, contohnya larutan asam kuat, basa kuat dan garam.
Dan elektrolit lemah yang memiliki daya hantar lemah, contohnya larutan jeruk, asam lemah, basa lemah.
Dan berikut contoh tabel larutan elektrolit kuat , elektrolit lemah dan non elektrolit dibawah ini :
Senyawa pembentuk larutan elektrolit
Senyawa pada larutan ini bisa menghantarkan arus listrik senyawa ion dan senyawa kovalen polar. Karena pada senyawa-senyawa tersebut bisa terionisasi ketika dilarutkan kedalam air.1. Senyawa ion
Senyawa ion disusun pada ion-ion yang memiliki bentuk padat dan kering. Ion-ion yang tersusun pada senyawa ion ketika pelarutannya akan bergerak bebas.Oleh karena itu larutan ion bisa menghantarkan arus listrik. Tetapi senyawa ion yang memiliki sebuah bentuk kristal, ion-ion berbentuk kristal tidak dapat bergerak bebas sehingga tidak akan bisa menghantarkan arus listrik. Contohnya pada senyawa ion yaitu NaCl, KCL, NaOH dan KOH.
2. Senyawa kovalen polar
Senyawa kovalen polar ketika dilarutkan kedalam air, akan langsung terurai menjadi ion-ion. Karena disebabkan pada ikatan kovalen senyawa tersebut mudah putus kedalam pelarut air dan akan menghasilkan ion-ion. Contoh yaitu asam klorida HCL, Amonia NH3.Contoh Larutan Elektrolit
1. Larutan elektrolit kuat
Larutan elektrolit kuat merupakan larutan yang molekulnya terurai menjadi sebuah ion-ion. Banyaknya ion-ion yang akan menghantarkan listrik pada bentuk ion yang disebut larutan elektrolit kuat.Contohnya pada larutan elektrolit kuat yaitu :
- Garam - NaCl, KCL, CuSO4, KNO3
- Asam Kuat - HCL, HI, HBr, H2SO4, HNO3
- Basa Kuat - NaOH, Ca(OH)2, Mg(OH)2, KOH
2. Larutan elektrolit lemah
Larutan elektrolit lemah merupakan larutan yang molekulnya tidak semuanya sempurna terionisasi. Karena itu molekul yang terurai menjadi ion-ion hanya sedikit yang bisa menghantarkan listrik.Contohnya pada larutan elektrolit lemah yaitu :
- Asam lemah - HCN, H3PO4, CH3COOH, dan C2O3
- Basa Lemah - NH4OH, Al(OH3) dan juga Fe(OH)3
3. Larutan non elektrolit
Untuk larutan yang satu ini adalah larutan yang tidak dapat menghantarkan sebuah arus listrik. Larutan pada non elektrolit berasal dari sebuah zat yang terurai kedalam air tetapi tidak berubah menjadi ion.Contoh larutan non elektrolit :
- Urea = CO (NH2)2
- Glukosa = C6H12O6
- Sukrosa = C12H22O11
- Etanol = C2H2OH
Baca Juga:
- Lampu Rumahmu Suka Mati Mendadak, Solusi Tepat Pengganti Lilin ini Wajib Kamu Coba
- Format Penyusunan dan Contoh Cover Makalah yang Benar
- Struktur dan Contoh Kata Pengantar Makalah yang Baik dan Benar
Ciri-ciri Larutan Elektrolit
1. Larutan elektrolit kuat
- Menghantarkan arus listrik yang kuat
- Terurai dengan sempurna
- Larutan elektrolit kuat memiliki derajat ion (A) A = 1
- Pada pengujiannya larutan elektrolit kuat memiliki nyala lampu yang sangat tenang dan memiliki gelembung gas banyak
2. Larutan elektrolit lemah
- Menghantarkan listrik yang lemah
- Tidak semuanya terurai
- Memiliki derajat ion A 0<A<1
- Pada pengujian larutan elektrolit lemah memiliki nyala lampu yang redup dan memiliki gelembung gas sedikit
3. Larutan non elektrolit
- Tidak bisa terurai
- Tidak bisa menjadi penghantar arus listrik
- Memiliki derajat ion (A) A = 0
- Pada pengujian larutan non elektronik. Lampu tidak dapat menyala dan gelembung gas tidak ada
Itulah pengertian dan contoh dari larutan elektronik dan non elektronik yang bisa membantu anda menambah pengetahuan larutan elektrolit dan non elektrolit.